Lactoferrine et assimilation du fer : une action complexe
Modifié le 14 décembre 2023
Temps de lecture : 7 minutes
•julienvenesson.fr ce n’est pas que des formations professionnelles en nutrition, la sélection des meilleurs livres et des consultations avec des nutritionnistes, c’est aussi les réponses à vos questions dans les articles du blog. Bonne lecture !•
Élément minéral indispensable à notre équilibre, le fer entre dans la composition de nombreuses protéines du corps humain. Son déficit, qui conduit à l’anémie, ou son excès, nocif en raison de son caractère oxydant, sont deux situations à éviter. Sa concentration est ainsi étroitement régulée dans l’organisme. La lactoferrine, un composé naturel, fait partie des acteurs impliqués dans ce phénomène.
Qu’est-ce que la lactoferrine ?
La lactoferrine est une protéine produite par le corps humain, au niveau de certaines cellules immunitaires, les neutrophiles, et par les glandes exocrines. Elle est ainsi présente dans les sécrétions comme le lait maternel, les larmes, la salive, le liquide synovial des articulations… Substance aux rôles multiples, elle exerce de nombreux bienfaits sur l’organisme.
Un membre de la famille des transferrines
La lactoferrine appartient à un groupe de protéines, les transferrines, qui partagent un point commun : leur capacité à se lier au fer. Une molécule de lactoferrine peut fixer deux ions ferriques (Fe3+). Contrairement aux autres transferrines qui relarguent facilement le fer de leur structure et jouent ainsi le rôle de transporteur, la lactoferrine ne s’en dissocie pas aisément. Elle est considérée comme une chélatrice de fer, une molécule capable de piéger l’élément minéral. Cette propriété lui confère un rôle antimicrobien : elle prive les pathogènes de cette source de subsistance. Sa tendance à rester unie au fer pourrait laisser penser que la prise de lactoferrine ne permet d’augmenter le stock de fer de l’organisme. Pourtant, elle participe activement à l’équilibre en fer.
Présence dans le lait maternel humain

La concentration la plus élevée de lactoferrine au sein des sécrétions du corps humain est relevée dans le lait maternel. Le colostrum, le premier lait produit pendant quelques jours après la naissance du bébé, en est particulièrement riche. Il contient 7g de lactoferrine par litre, un taux qui décline ensuite progressivement pour se stabiliser à environ 2g/L dans le lait mature. Il s’agit d’une exception chez les mammifères, le lait des autres espèces en est plus pauvre.
Cette présence massive de lactoferrine pourrait expliquer la haute biodisponibilité du fer contenu dans le lait maternel. On estime en effet qu’il est assimilé à hauteur de 50%, contre moins de 12% pour le fer des laits infantiles. Ainsi, malgré la faible teneur en fer du lait maternel, de l’ordre de 0,2 à 0,4mg/L, les bébés allaités sont moins exposés aux carences que les bébés nourris avec des préparations pour nourrissons durant leurs premiers mois de vie.
L’intestin des nourrissons est conçu pour aborder la lactoferrine
Les nouveau-nés présentent une singularité : ils possèdent un récepteur spécifique de la lactoferrine en grande quantité au niveau de leurs cellules intestinales. Si ce récepteur existe toujours à l’âge adulte, il est réparti différemment dans l’organisme, présent au niveau de nombreux tissus (cœur, muscles, pancréas…) et moins concentré dans l’intestin. La lactoferrine du lait maternel se lie à ce récepteur puis est absorbée par les cellules qui tapissent l’organe, les entérocytes. Le fer en est extrait, et devient disponible pour l’organisme. Comme entre 20 et 45% du fer présent dans le lait maternel est lié à la lactoferrine, ce mécanisme aide l’enfant à couvrir ses besoins martiaux. Il complète la captation classique du fer par les entérocytes.
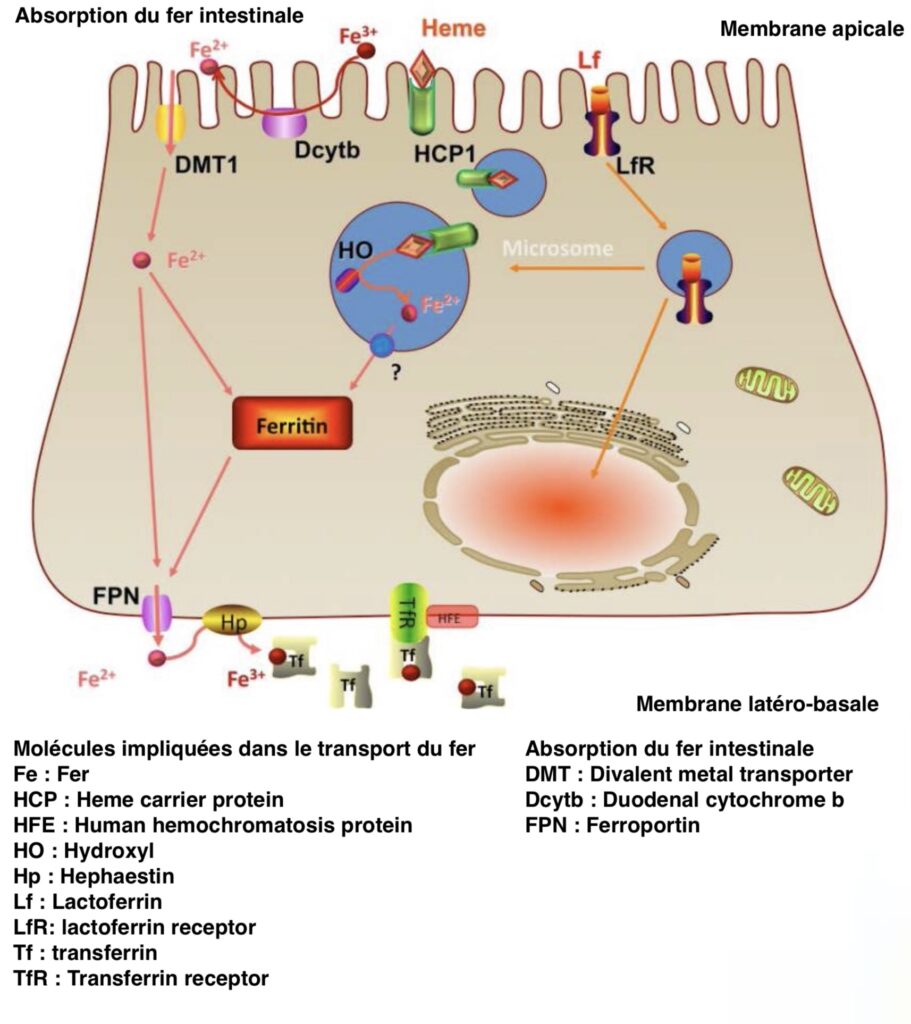
La lactoferrine augmente l’absorption du fer
La lactoferrine apparaît en mesure d’améliorer la quantité de fer assimilée au cours du repas. Des chercheurs ont conduit une expérience auprès de bébés de 4 mois. Les enfants ont reçu une bouillie à base de farine de maïs, enrichie en sulfate ferreux. Dans une partie des tests, ils ont ajouté de la lactoferrine. Ils ont ensuite évalué la quantité de fer assimilée par l’enfant. En l’absence de lactoferrine, 6,3% du fer provenant du sulfate ferreux a été absorbé. En présence de lactoferrine, le taux d’absorption est passé à 9,8%, soit une augmentation de 56%. La lactoferrine ajoutée à la bouillie a capté une partie de fer et l’a rendue disponible pour son absorption intestinale par l’intermédiaire de son récepteur.
Cette optimisation de l’assimilation du fer a également été mise en évidence lors d’une étude menée auprès de bébés de 4 à 6 mois recevant une préparation pour nourrissons enrichie en fer. Le statut en fer des bébés s’est amélioré, mais uniquement quand la formule contenait en plus de la lactoferrine.
Rôles de la lactoferrine chez l’adulte
Chez l’adulte, la lactoferrine reste cruciale pour bénéficier d’un bon équilibre en fer. Ses bienfaits passent alors essentiellement par ses propriétés anti-inflammatoires. Elles permettent de préserver l’efficacité d’un système régulant la circulation du fer entre les cellules intestinales et le reste de l’organisme.
Le duo ferroportine-hepcidine régule l’arrivée du fer
Quand le fer présent dans les aliments que nous consommons est prélevé par les entérocytes, il peut être stocké sous forme de ferritine si la demande de l’organisme est faible.
S’il existe un besoin important, pour fabriquer des globules rouges par exemple, il doit en être exporté. Il va alors simplement traverser l’entérocyte puis gagner la circulation sanguine pour être acheminé là où il est attendu. Il emprunte une porte de sortie formée par une protéine, la ferroportine. Comme l’excès de fer est toxique, ce mécanisme est étroitement régulé pour éviter un afflux trop massif dans le sang.
Lorsque des stocks importants de fer s’accumulent au niveau du foie, l’organe déclenche la production d’un petit composé, l’hepcidine. Celle-ci va alors se fixer sur la ferroportine, ce qui provoque son absorption par l’entérocyte en vue de sa dégradation. Le fer qui entre dans l’entérocyte ne peut dès lors plus en sortir. À mesure que l’organisme puise dans son stock de fer hépatique pour satisfaire ses besoins, la production d’hepcidine décline. La neutralisation de la ferroportine est levée, l’exportation du fer reprend.
La disponibilité du fer est mise à mal par les phénomènes inflammatoires
Ce phénomène de régulation sophistiqué permet d’éviter le déficit ou l’excès de fer dans l’organisme. Cette machinerie peut cependant s’enrayer. Lors de certaines situations pathologiques, les niveaux d’inflammation s’élèvent. Des messagers inflammatoires comme les interleukines 6, 1α et 1β vont alors provoquer une surproduction d’hepcidine.
Le fer reste en conséquence séquestré à l’intérieur des cellules. Ce phénomène est en fait une réponse efficace du corps en cas d’agression par des pathogènes. En limitant la quantité de fer présente dans le milieu extracellulaire, les microbes qui en ont besoin pour se développer ne peuvent plus prospérer.
L’anémie inflammatoire

En cas d’infection aiguë, la situation revient en général rapidement à la normale et l’équilibre en fer est vite rétabli. En revanche, lorsque l’inflammation se prolonge, dans le cadre de maladies chroniques ou du surpoids, l’organisme vient à manquer de fer. Augmenter ses apports externes reste vain : les cellules intestinales ne sont pas privées d’approvisionnement, mais le minéral y reste prisonnier. La production d’hémoglobine, la molécule chargée du transport de l’oxygène au sein des globules rouges, est altérée. Une anémie d’origine inflammatoire se développe, avec les signes typiques de cette situation associant fatigue, essoufflement et pâleur.
La lactoferrine peut contrer l’anémie inflammatoire
La lactoferrine apparaît en mesure de résoudre le problème, car elle agit à sa source. Des travaux conduits en laboratoire ont permis de rendre compte des effets de l’ajout de lactoferrine bovine sur des cultures de macrophages, un type de globules blancs.
La structure chimique et les propriétés de la lactoferrine bovine et de la lactoferrine humaine sont très proches. Les analyses ont révélé que la lactoferrine parvient à diminuer la production des messagers inflammatoires et ainsi à préserver l’activité de la ferroportine. Le pouvoir anti-inflammatoire de la lactoferrine, plus que son contenu en fer, peut donc représenter un moyen de lutter contre l’anémie. Des essais cliniques ont été menés chez l’être humain pour évaluer la fiabilité de cette piste.
Rôle dans le traitement de l’anémie ferriprive
L’anémie ferriprive est une situation fréquente, qui affecte une personne sur trois à travers le monde. Les femmes enceintes et les enfants y sont particulièrement exposés. La prise en charge médicale classique de cette situation, qui repose sur l’administration de sulfate ferreux, n’est pas toujours efficace et comporte des effets indésirables. La lactoferrine apparaît comme une alternative intéressante.
Amélioration du statut en fer
Des chercheurs ont récemment analysé les résultats de 11 études évaluant les effets de la supplémentation en lactoferrine en cas d’anémie ferriprive, par rapport à l’administration de sulfate ferreux. Ils ont mis en évidence la supériorité de la lactoferrine, qui parvient à améliorer le taux de fer sanguin, de ferritine et la concentration en hémoglobine plus efficacement que le sulfate de fer.
De plus, si la lactoferrine réduit la production d’interleukine-6, le sulfate ferreux l’augmente. On comprend aisément que l’administration de ce dernier se solde souvent par un échec, puisqu’il entretient un des mécanismes à l’origine de l’anémie.
Un effet marqué chez les enfants et les femmes enceintes
La capacité de la supplémentation en lactoferrine à combattre l’anémie a été mise en évidence chez des personnes de toutes conditions. Dans l’analyse précédente, les études portaient sur des adultes, majoritairement des femmes enceintes. Les effets positifs concernent également les plus jeunes. Une étude menée auprès d’enfants de 6 à 12 ans souligne son efficacité pour améliorer les paramètres sanguins liés au fer en complémentation sur 30 jours. Chez des bébés de 8 mois, elle améliore non seulement l’hématocrite – une valeur qui représente la proportion des globules rouges dans le sang – mais diminue également le risque infectieux.
Un soutien pour les malades du cancer
Les personnes souffrant de cancer développent souvent une anémie en raison de l’intensité des phénomènes inflammatoires qui sévissent dans leur organisme. Ils sont liés à la maladie elle-même et aux traitements de radiothérapie ou chimiothérapie. En combinaison avec les traitements classiques, la lactoferrine administrée par voie orale s’avère efficace dans ce cadre, et pourrait se substituer à l’administration de gluconate ferreux par voie intraveineuse.
Quand faut-il prendre la lactoferrine ?
Une étude souligne l’importance des modalités de la prise de lactoferrine pour obtenir un bon résultat contre l’anémie. Des femmes enceintes ont bénéficié de 100mg de lactoferrine 2 fois par jour. Dans un premier groupe, le traitement était pris avant le repas, dans le second pendant le repas. Seules les femmes du premier groupe ont vu leur statut en fer s’améliorer. Les enzymes digestives peuvent dégrader la lactoferrine et entraîner une baisse d’efficacité. Il est donc nécessaire de prendre la lactoferrine à distance du repas.
Tolérance digestive
La supplémentation en lactoferrine présente par ailleurs un autre atout par rapport aux suppléments de fer : elle est mieux tolérée par l’organisme. L’administration de sulfate ferreux provoque en effet souvent des troubles gastro-intestinaux comme des nausées ou vomissements, et un inconfort dans la région de l’estomac. Ces désagréments conduisent bon nombre de personnes à stopper leur traitement. De plus, un excès de fer augmente le risque d’infection chez l’enfant.
Autres articles




