Quels sont les oxydants retrouvés dans le corps humain ?
Modifié le 15 décembre 2023
Temps de lecture : 8 minutes
•julienvenesson.fr ce n’est pas que des formations professionnelles en nutrition, la sélection des meilleurs livres et des consultations avec des nutritionnistes, c’est aussi les réponses à vos questions dans les articles du blog. Bonne lecture !•
Notre organisme produit naturellement des molécules oxydantes, parmi lesquelles se trouvent les fameux radicaux libres, connus pour générer du stress oxydatif. Mais quelles sont les différentes molécules oxydantes présentes dans notre corps et comment influencent-elles notre santé ?
Notre organisme contient de nombreuses molécules oxydantes
Par définition, un oxydant est une molécule qui peut fournir de l’oxygène et fixer des électrons. Dans l’organisme, le stress oxydant est lié à la présence des espèces réactives de l’oxygène (ERO, ou ROS en anglais). Toutes les espèces réactives ne sont pas des radicaux libres, mais les radicaux libres font partie des espèces réactives et représentent même une part importante des ERO. Un radical libre est un atome ou une molécule qui possède au moins un électron célibataire (non-apparié), ce qui le rend instable et très réactif.
Notre consommation d’oxygène favorise la production des ERO
Les ERO sont des sous-produits du métabolisme aérobie. Elles sont produites surtout au niveau des mitochondries, à cause de la respiration cellulaire. La réduction de l’oxygène moléculaire en eau est catalysée par la dernière enzyme de la chaîne respiratoire, la cytochrome oxydase.
Parmi les ERO se trouvent :
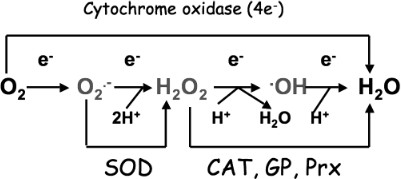
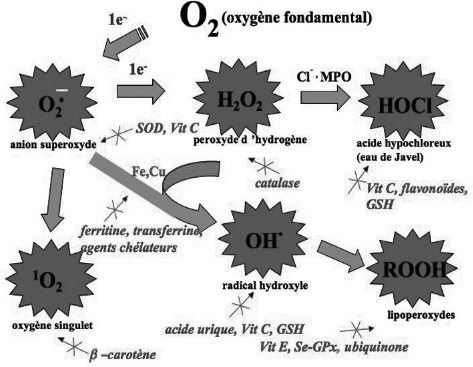
- l’anion superoxyde O2•– formé lors de la réduction d’O2 pendant la respiration mitochondriale. Cet anion est un radical libre qui permet de produire d’autres ERO. Les systèmes enzymatiques qui interviennent dans sa formation sont la NADPH oxydase de la membrane et la cytochrome oxydase de la chaîne respiratoire ;
- le radical hydroxyle •OH, qui est une espèce très toxique et très réactive. Il peut être produit par différentes voies, par exemple par la décomposition de H2O2 en présence de métaux, comme les ions ferreux Fe2+, par la réaction de Fenton ;
- le peroxyde d’hydrogène H2O2, qui est produit par la dismutation de l’anion superoxyde par la superoxyde dismutase. Il peut être éliminé en O2 et H2O, grâce à l’intervention de la catalase. Contrairement aux deux ERO précédentes, le peroxyde d’hydrogène n’est pas un radical libre, il est plus stable, mais permet quand même la formation d’autres ERO. Chez l’homme, il existe une trentaine d’oxydases cellulaires qui peuvent produire du peroxyde d’hydrogène ;
- l’oxygène singulet 1O2, produit sous l’action des ultraviolets sur le dioxygène, notamment au niveau de la peau, ce qui favoriserait son vieillissement, ainsi que des cancers ;
- les radicaux peroxyles formés par oxydation des membranes…
Les espèces réactives de l’azote agissent avec les ERO
Nous produisons aussi des espèces réactives de l’azote, parmi lesquelles se trouvent :
- le monoxyde d’azote NO•, qui provient d’une réaction catalysée par la NO synthase avec un azote de l’acide aminé arginine. Le monoxyde d’azote peut générer des ions nitrites ;
- l’ion peroxynitrite ONOO-, issu de la réaction entre NO• et O2•–.
Ces espèces réactives de l’azote agissent souvent en synergie avec les ERO pour générer un stress oxydant et nitrosant.
Le fer et les métaux lourds sont pro-oxydants
Le fer est un élément indispensable au bon fonctionnement de l’organisme car il intervient comme cofacteur de nombreuses réactions biologiques. Il est indispensable au transport de l’oxygène dans les globules rouges.
Mais l’accumulation de fer dans les tissus aggrave la production des ERO. En effet, il participe aux réactions redox qui génèrent des ERO et contribue au stress oxydatif. En particulier, les ions ferreux sont des catalyseurs de la réaction de Fenton qui produit des radicaux hydroxyle. Or ces radicaux sont très toxiques. En ce sens, les cellules doivent maintenir une certaine homéostasie du fer afin de se prémunir du stress oxydant.
Par ailleurs, les métaux lourds (plomb, mercure…) sont des toxiques pour l’organisme car ils génèrent des espèces réactives de l’oxygène et de l’azote, ce qui provoque un stress oxydatif. Une exposition à long terme à ces métaux conduit à l’apoptose (la mort cellulaire programmée) des cellules.
L’alimentation peut apporter des molécules oxydantes
L’alimentation peut être pro-oxydante, notamment si elle apporte des quantités importantes d’alcool ou d’aliments sucrés. En effet, l’hyperglycémie génère un stress oxydant. Cela serait lié à l’oxydation du glucose, mais aussi aux réactions de glycation. Ces réactions fixent un glucose sur la fonction amine d’une protéine et donnent des produits de glycation avancés (AGE pour advanced glycation endproducts). Les AGE peuvent également provenir de l’oxydation des graisses.
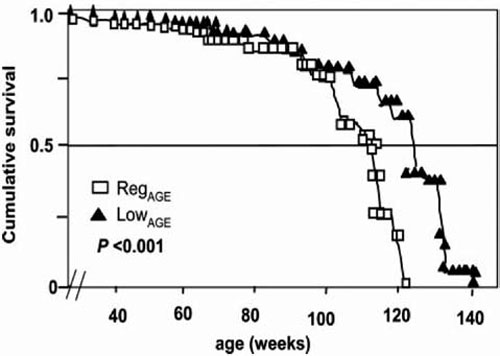
Les AGE se forment naturellement dans le corps, mais ils peuvent aussi être apportés par l’alimentation. En cuisine, des AGE se forment lors de la cuisson, par réaction entre des sucres et des protéines, ce qui donne aux aliments une coloration dorée. Les viandes grillées, les aliments trop cuits, apportent des AGE. Or les AGE se fixent sur des récepteurs cellulaires et favorisent la formation de radicaux libres. Ils sont pro-oxydants. En réduisant ses apports alimentaires en AGE, on peut diminuer le stress oxydant de l’organisme.
Et l’homocystéine ?
L’homocystéine est une source d’oxydation pour l’organisme. Lors d’analyses sanguines, l’augmentation de son taux prédispose à des troubles cardiovasculaires. L’auto-oxydation de l’homocystéine produit des ERO qui stimulent la peroxydation des lipides et la production de dérivés AGE, qui peuvent favoriser des plaques d’athérome.
L’homocystéine provient du métabolisme des acides aminés soufrés.
L’organisme recherche l’équilibre entre oxydants et antioxydants
L’organisme dispose de défenses antioxydantes naturelles pour limiter les dommages que pourraient créer les oxydants. Notre potentiel antioxydant dépend de nos habitudes de vie.
L’accumulation de radicaux libres favorise le stress oxydant
Lorsque l’organisme est dépassé par une production trop importante de radicaux libres, on parle de stress oxydant. Les ERO deviennent alors toxiques, favorisent le vieillissement cellulaire ainsi que des pathologies.
Logiquement, plus notre consommation d’oxygène augmente, plus la production d’ERO s’accroît. C’est ce qui se passe lors d’un effort physique. Le sport génère donc un stress oxydant pour l’organisme. Cependant la respiration n’est pas le seul processus à l’origine du stress oxydant, les stress environnementaux étant aussi impliqués : consommation d’alcool, tabagisme, pollution, exposition au soleil…
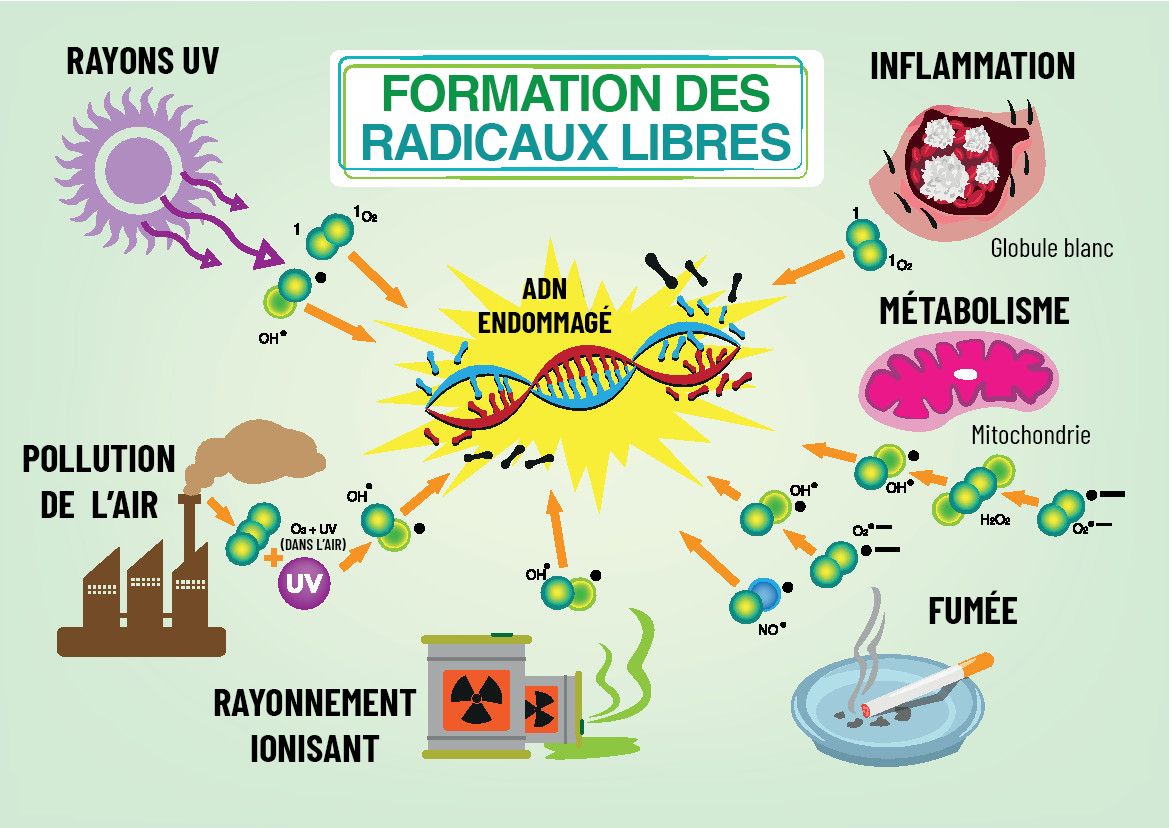
Les ERO peuvent s’avérer toxiques pour l’organisme
Dans son Guide des aliments antioxydants, Juliette Pouyat-Leclère explique que les ERO « attaquent tous les matériaux biologiques (ADN, protéines, lipides…). » Par exemple les ERO « provoquent des cassures et des mutations au sein de l’ADN, initiant ainsi la cancérogénèse ; elles dénaturent et inactivent les protéines (oxydation des acides aminés, fragmentation de polypeptides…) ; elles oxydent les sucres (glucose) ; elles dégradent les lipides membranaires et altèrent ainsi la perméabilité des membranes cellulaires. »
Les espèces réactives de l’oxygène attaquent tous les matériaux biologiques
Plus précisément, les ERO agissent sur :
- les acides nucléiques : le radical hydroxyle est particulièrement toxique. Les radicaux libres oxydent les bases azotées, en particulier la guanine, qui est transformée en 8-hydroxyguanine ;
- les protéines et les acides aminés, qui peuvent être oxydés par les ERO. Les acides aminés soufrés (comme la cystéine), basiques ou aromatiques sont les plus sensibles à cette oxydation. Cela a pour conséquence d’altérer les protéines et donc leur fonctionnement ;
- les lipides des membranes : les ROS conduisent à la peroxydation des lipides, ce qui altère les membranes lipidiques et peut conduire à la mort cellulaire.
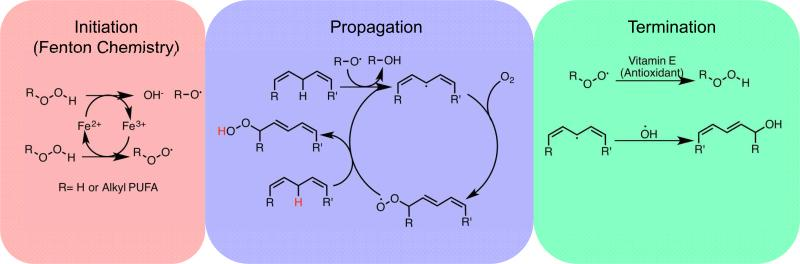
Notre organisme possède des défenses antioxydantes
Pour se défendre contre ces ERO potentiellement toxiques, l’organisme a développé des défenses antioxydantes, notamment grâce à des enzymes : la superoxyde dismutase, la catalase et la glutathion peroxydase. Des antioxydants apportés par l’alimentation peuvent aussi contribuer à la lutte contre les radicaux libres.
Pour connaître son statut oxydant, il est possible de faire un bilan sanguin dans un laboratoire d’analyses spécialisé. Le bilan s’appuie sur la concentration en enzymes antioxydantes (superoxyde dismutase, glutathion peroxydase…), des oligo-éléments nécessaires au fonctionnement de ces enzymes (sélénium, cuivre), du fer (catalyseur de la formation des ERO), de la vitamine C (antioxydante) et des marqueurs de l’oxydation : des molécules issues des dommages réalisés par les ERO. Par exemple, les lipides peroxydés, les protéines oxydées constituent des marqueurs du stress oxydatif.
Cependant un stress oxydant modéré ou une production très localisée de radicaux libres participent aussi au bon fonctionnement de l’organisme.
Les oxydants jouent des rôles essentiels dans l’organisme
À ce stade il est important de noter que les ERO sont souvent produites dans des compartiments particuliers des cellules (mitochondries, vésicules de phagocytose…). Cette compartimentation explique qu’elles ne sont pas forcément toxiques, dans la mesure où leur production est localisée dans un compartiment bien particulier. Ainsi, l’accumulation de radicaux libres dans la matrice d’une mitochondrie n’a pas le même effet que si elle a lieu dans le cytosol de la cellule.
Les ERO participent à la transduction de messages cellulaires
De petites quantités d’ERO jouent le rôle de signaux dans les cellules et permettent le maintien des fonctions physiologiques. Elles interviennent dans un processus appelé « biologie redox ». Au cours de l’évolution, la nature aurait sélectionné les ERO comme mécanisme de transduction du signal pour permettre l’adaptation à des changements environnementaux.
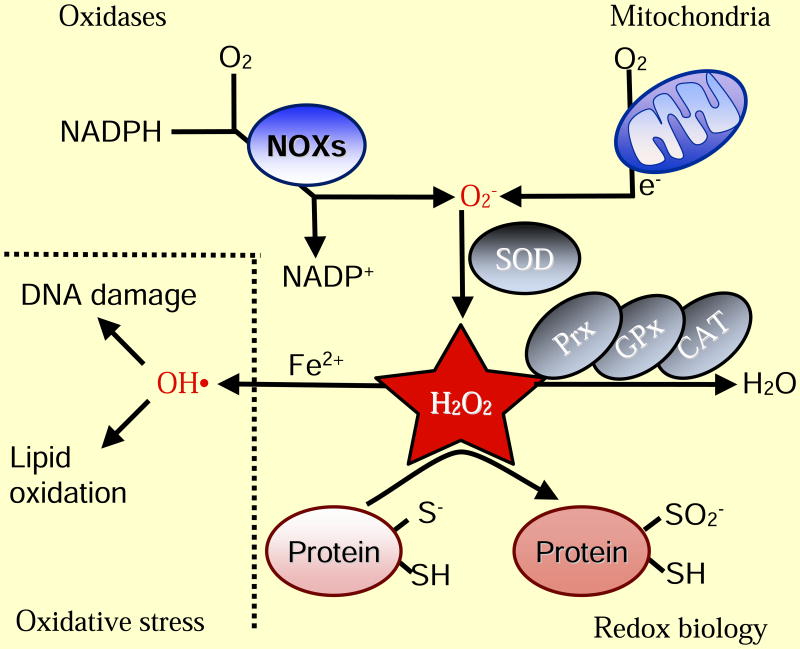
Par exemple, le peroxyde d’hydrogène peut oxyder des résidus cystéine des protéines, ce qui modifie la structure des protéines et donc leur activité. L’oxydation de certaines cystéines essentielles peut abolir une activité phosphatase et avoir une incidence sur la transduction du signal intracellulaire. L’oxydation des cystéines peut être considérée comme un signal.
Les radicaux libres sont aussi des messagers qui influencent l’expression des gènes.
Le sport génère des ERO
L’effet bénéfique d’un petit stress oxydant se voit tout particulièrement dans le cas de l’activité physique. L’exercice augmente la production des ERO et active des voies biologiques favorables à la santé, ce qui explique qu’il améliore la longévité et réduit le risque de diabète de type 2.
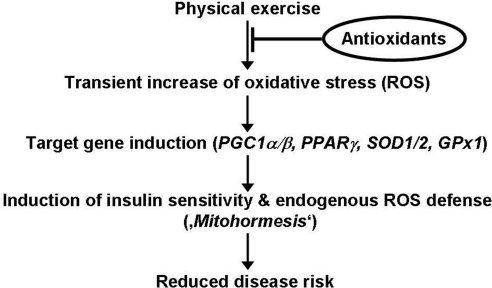
Cet effet bénéfique du stress oxydatif a été démontré dans une expérience parue en 2009. Des chercheurs allemands ont recruté 39 jeunes hommes en bonne santé, qui ont suivi un programme d’exercice de quatre semaines. Certains ont été complémentés en antioxydants (vitamines C et E) et d’autres ont eu un placebo. L’expérience a montré que l’exercice améliore la sensibilité à l’insuline, mais seulement en l’absence d’antioxydants. Cela s’accompagnait par une augmentation de l’expression de régulateurs de la sensibilité à l’insuline sensibles aux ERO. L’exercice favorisait également les défenses antioxydantes naturelles de l’organisme : superoxyde dismutase et glutathion peroxydase. Mais cet effet était bloqué par les compléments d’antioxydants.
Les auteurs en concluent que « le stress oxydatif induit par l’exercice améliore la résistance à l’insuline et provoque une réponse adaptative favorisant la capacité de défense antioxydante endogène. »
Le stress oxydatif induit par l’exercice […] provoque une réponse adaptative favorisant la capacité de défense antioxydante endogène
Ce mécanisme peut s’expliquer par le principe de l’hormèse. L’hormèse fait référence à des réponses adaptatives des systèmes biologiques à des défis environnementaux modérés ou auto-imposés grâce auxquels l’organisme améliore sa tolérance à des défis plus sévères. Cela signifie qu’un défi environnemental qui induit un stress oxydatif modéré peut avoir un effet protecteur à long terme car l’organisme saura mieux se protéger plus tard d’un stress plus important.
Pour le Dr Mark Mattson, expert dans le vieillissement du cerveau, « L’hormèse est un concept fondamental de la théorie de l’évolution. Depuis le début jusqu’à nos jours, la vie sur terre a existé dans des environnements difficiles dans lesquels les cellules sont souvent exposées aux radicaux libres et aux substances toxiques. Pour éviter l’extinction, les organismes ont développé des mécanismes complexes pour faire face aux risques environnementaux. » Cette résistance au stress s’acquiert grâce à l’action de différentes protéines, en particulier les enzymes antioxydantes.
La production des ERO intervient dans l’immunité
Les ERO participent aux défenses de l’organisme contre des agressions extérieures. Par exemple, au niveau du système immunitaires, les radicaux libres servent à la destruction d’agents pathogènes dans le cadre de la phagocytose.
Ainsi, dans les macrophages, les phagosomes contiennent des quantités importantes d’ERO qui attaquent l’agent phagocyté (bactérie par exemple), entraînant sa destruction. Ces grandes quantités d’ERO sont produites grâce aux enzymes NADPH oxydases (NOX), qui réduisent l’oxygène O2 en ion superoxyde.
En conclusion, les molécules oxydantes produites par la respiration cellulaire jouent des rôles dans l’adaptation de l’organisme. Elles deviennent nocives quand nos défenses antioxydantes naturelles sont dépassées.
Autres articles



