Les myokines : l’hormone de jouvence produite par nos muscles
Modifié le 19 décembre 2023
Temps de lecture : 10 minutes
•julienvenesson.fr ce n’est pas que des formations professionnelles en nutrition, la sélection des meilleurs livres et des consultations avec des nutritionnistes, c’est aussi les réponses à vos questions dans les articles du blog. Bonne lecture !•
Lorsque nous pratiquons une activité sportive, nos muscles produisent de petites molécules encore méconnues : les myokines. Ces substances sont en réalité des hormones en mesure d’activer des fonctions clés au sein des cellules de tout notre organisme. Certaines myokines ont notamment des effets anti-âge documentés.
Que sont les myokines ?
La pratique sportive régulière exerce de multiples bienfaits sur notre santé, diminuant le risque de développer des maladies chroniques ou leur intensité, et la mortalité de façon générale. Les mécanismes biologiques permettant ces effets ont longtemps été partiellement compris. Aujourd’hui les recherches indiquent un rôle très important des myokines dans la médiation de ces effets.
Les myokines sont de petites protéines sécrétées par les fibres musculaires lorsqu’elles se contractent. Elles agissent sur le muscle lui-même (action autocrine) et les tissus qui l’environnent (action paracrine), elles sont également relarguées dans la circulation sanguine. Elles exercent ainsi des effets sur des organes plus éloignés comme le foie, les reins, le cerveau, les os, l’intestin… Le muscle peut ainsi être qualifié d’organe sécréteur en raison de cette action hormonale.
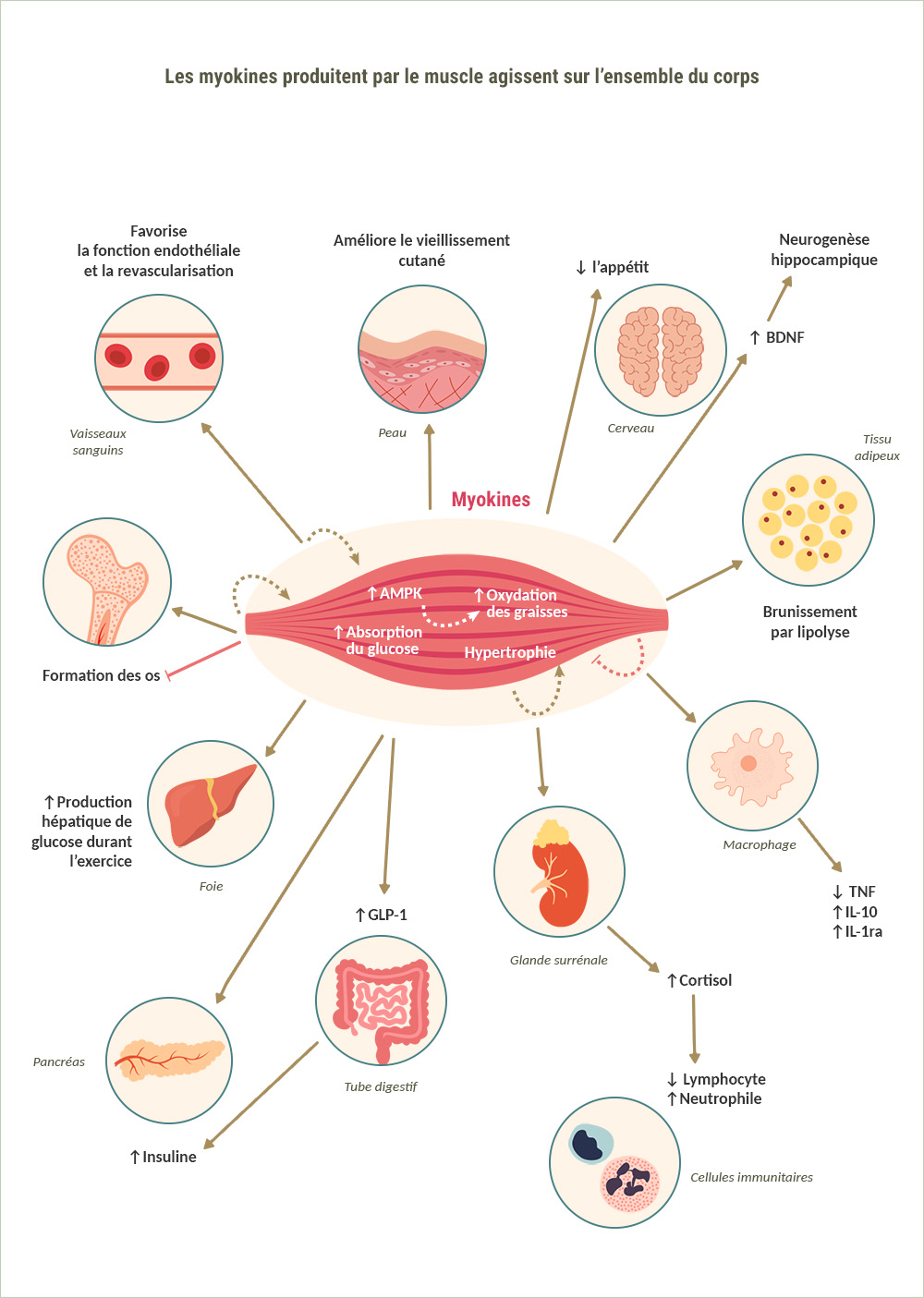
Un très grand nombre de myokines
Le terme myokine a été introduit pour la première en 2003 par un chercheur suédois, Bengt Saltin. À ce jour, plus de 650 myokines ont été identifiées. Leur rôle reste encore mal connu : les fonctions spécifiques de seulement 5% d’entre elles ont été caractérisées.
Les myokines les plus étudiées sont les interleukines 6, 8, 10, 13, 15 et 18, ainsi que la muscline, l’irisine, le facteur de croissance des fibroblastes 21 (FGF21), la myostatine, la myonectine ou encore l’apéline. Elles pourraient avoir des applications thérapeutiques dans le cadre des troubles du métabolisme, car leur dérégulation en cas de sédentarité est propice à la survenue de l’obésité et du diabète de type 2.
Des effets anti-âge prometteurs
Le champ de la médecine anti-âge s’intéresse également de près à ces composés. En effet, la sécrétion de la plupart des myokines s’amenuise au fil des années, ce qui pourrait contribuer au vieillissement de l’organisme. Par exemple :
- La longueur de l’extrémité des chromosomes, généralement considérée comme un bon marqueur de l’âge biologique, est par exemple corrélée au taux d’irisine.
- L’interleukine 15 quant à elle apparaît cruciale contre le vieillissement de la peau. L’administration d’IL-15 à des souris âgées, tout comme l’exercice physique, améliore le contenu de l’épiderme et du derme en collagène.
Effet anti-âge sur les muscles
Au cours du vieillissement, la masse musculaire et la force diminuent. Lorsque la situation devient critique, on parle de sarcopénie. Une étude impliquant des chercheurs français de l’INSERM a mis en lumière le rôle clef d’une des myokines, l’apéline, dans ce phénomène qui représente un facteur de la fragilité pour les aînés.
Baisse de l’apéline avec l’âge
Si la pratique d’une activité sportive élève la concentration sanguine en apéline, le mécanisme s’émousse avec l’âge, comme l’ont mis en évidence les chercheurs.
Ils ont tout d’abord analysé la concentration sanguine en apéline chez des souris à différentes étapes de leur vie : à l’âge de 3, 12 et 24 mois. Les résultats ont souligné une baisse progressive à mesure de l’avancée en âge des animaux. Cette baisse du taux sanguin d’apéline est associée à une raréfaction du composé lui-même, et de ses récepteurs, au niveau musculaire.
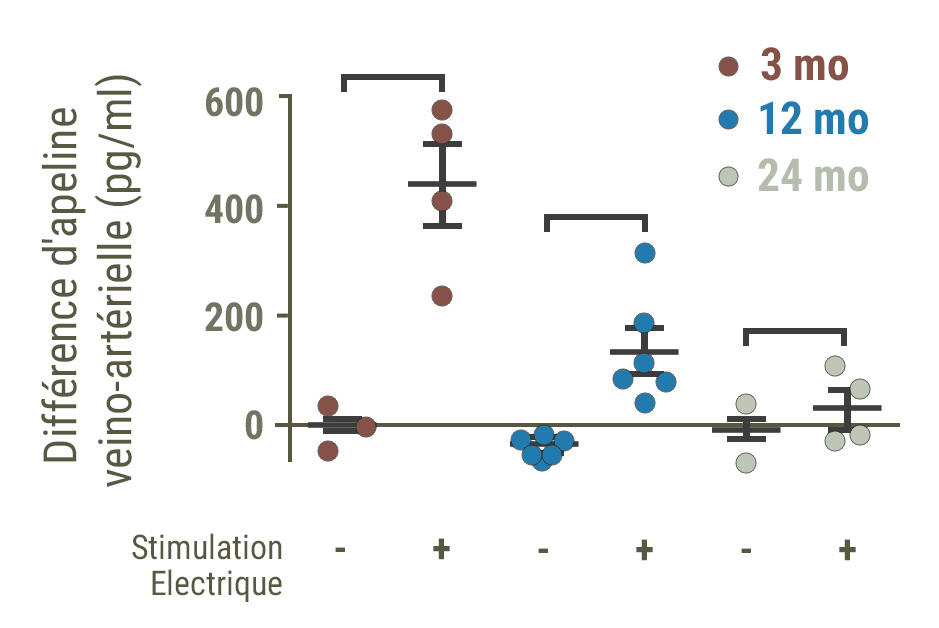
Lorsque les muscles des jeunes souris ont été stimulés pour imiter une activité physique, ils ont produit une quantité plus élevée d’apéline par rapport à ce qui a été observé chez leurs congénères âgées.
L’équipe a ensuite voulu vérifier si ces résultats étaient transposables à l’être humain. Ils ont pour cela utilisé des cultures de cellules musculaires provenant de donneurs âgés (68 à 83 ans) et plus jeunes (16 à 27 ans). Là encore, la perte du contenu en apéline au cours du vieillissement a été mise en évidence, ainsi que la baisse de réactivité des cellules musculaires à produire ce composé.
Effet anti-catabolisant de l’apéline
Les chercheurs se sont ensuite penchés sur la manière dont le système musculaire des animaux privés de l’action de l’apéline évoluait au cours du vieillissement.
Ils ont pour cela utilisé une souche de souris déficiente en apéline ou en ses récepteurs. Dans les deux cas, le résultat est le même : l’organisme ne peut profiter des effets du composés. Ils ont constaté les muscles de ces animaux s’altéraient bien plus précocement que ceux de leurs congénères.
L’apéline rajeunit les muscles
Afin de démontrer de manière incontestable le rôle de l’apéline en tant que source de rajeunissement musculaire, une étape finale a été entreprise : l’administration de ce composé à des animaux âgés. L’approche a permis d’inverser la sarcopénie, conduisant à une augmentation significative de la masse musculaire et de la proportion de fibres de grand diamètre.
Plusieurs mécanismes conduisant à cette restauration de l’intégrité des muscles ont été identifiés. L’apéline a stimulé la formation de nouvelles mitochondries, les unités de production d’énergie, et a favorisé la synthèse des protéines au sein des fibres musculaires sarcopéniques. De plus, elle a augmenté la quantité de cellules souches musculaires et leur capacité à proliférer et à fusionner pour régénérer les muscles endommagés.
Des travaux antérieurs avaient montré que les effets anti-âge de l’apéline s’étendent au-delà de la sphère musculaire. Son administration avait freiné le vieillissement global de l’organisme de souris et prolongé leur espérance de vie.
Une coopération de myokines contre la sarcopénie
D’autres myokines exercent des effets favorables pour prévenir le vieillissement musculaire :
- L’irisine induit elle aussi la régénération des muscles en activant les cellules souches.
- Le FGF21 prévient l’atrophie musculaire provoquée par les états inflammatoires, souvent présents chez les personnes âgées.
- La météorine-like favorise la formation de nouveau tissu musculaire.
- L’IGF-1 est une myokine essentielle pour la croissance des muscles et leur régénération. De faibles niveaux de cette myokine sont associés à un risque accru de sarcopénie.
En augmentant la sécrétion de ces myokines, l’exercice physique chez les personnes âgées peut ainsi contribuer au maintien de la fonction musculaire, réduisant le risque de chutes et de fractures qui conduisent souvent à la perte d’autonomie.

Effet anti-âge sur le cerveau
Les myokines pourraient par ailleurs représenter un moyen de freiner le vieillissement cérébral et de maintenir les capacités mentales au fil des années.
Prévenir le déclin des facultés mentales
Le sport exerce des effets favorables sur la santé cérébrale et les fonctions cognitives, tout particulièrement au sein de la population âgée.
Une méta-analyse a démontré le rôle central de l’activité physique dans la lutte contre le déclin cognitif lié au vieillissement. Elle a synthétisé les données de 15 études, ayant porté sur près de 34 000 personnes non démentes, suivies pendant 1 à 12 ans. Au cours de cette période, 3210 cas de baisse des capacités mentales ont été recensés.
Les personnes les plus actives sur le plan physique avaient un risque réduit de 38% d’en être affectées. Celles qui maintenaient un niveau d’activité faible à modéré étaient également protégées, avec un risque réduit de 35% par rapport aux inactifs.
Le sport fait également partie des approches permettant de réduire le risque de développer une affection neurodégénérative comme la maladie d’Alzheimer et de Parkinson, ou d’en atténuer les signes.
Le BDNF, médiateur des bienfaits du sport sur le cerveau
Plusieurs mécanismes peuvent expliquer les bienfaits du sport sur le cerveau. L’exercice physique améliore la circulation sanguine et l’apport en oxygène au sein des tissus cérébraux, réduit les niveaux de stress et d’inflammation… Mais ce ne sont pas les seuls facteurs en jeu. Il agit également sur la production d’un composé essentiel pour la sphère cérébrale, le facteur neurotrophique issu du cerveau (BDNF).
Le BDNF est un membre majeur de la famille des neurotrophines, des protéines responsables de la croissance, de la survie et de la différenciation des cellules appartenant au système nerveux. Au niveau du cerveau, les plus hauts niveaux de BDNF sont rencontrés dans les neurones de l’hippocampe, une région impliquée dans les phénomènes d’apprentissage et de mémorisation. Il est également présent en quantité importante dans l’amygdale, le cervelet et le cortex cérébral.
Protection et formation de nouveaux neurones
Le BDNF exerce ses effets bénéfiques en se liant à un récepteur présent en surface des neurones, le récepteur tyrosine kinase (TrkB). Il déclenche alors des cascades de réactions au sein de ceux-ci. L’une des voies activées – la voie de signalisation Ras/MAPK/ERK – est impliquée dans la neurogenèse, notamment grâce à l’activation de facteurs de transcription appelés CREB.
La capacité à former de nouveaux neurones à partir de cellules souches persiste en effet à l’âge adulte dans certaines régions du cerveau, en particulier dans l’hippocampe. Ce phénomène est important pour le maintien des fonctions cérébrales au cours du temps.
Le BDNF favorise également par ce biais le développement des structures qui permettent aux neurones de communiquer les uns avec les autres, les axones et les dendrites. Il contribue ainsi à la plasticité cérébrale, cette aptitude du cerveau à modifier les connexions entre ses neurones pour effectuer de nouveaux apprentissages ou récupérer après un traumatisme.
Le BDNF joue également un rôle protecteur, favorisant la survie des neurones par l’intermédiaire de la voie de signalisation IRS-1/PI3K/AKT. Elle conduit à la neutralisation de composés qui favorisent la mort cellulaire comme le facteur de transcription Forkhead ou les protéines BAD. Ces dernières ont récemment été incriminées dans le développement de la maladie d’Alzheimer.
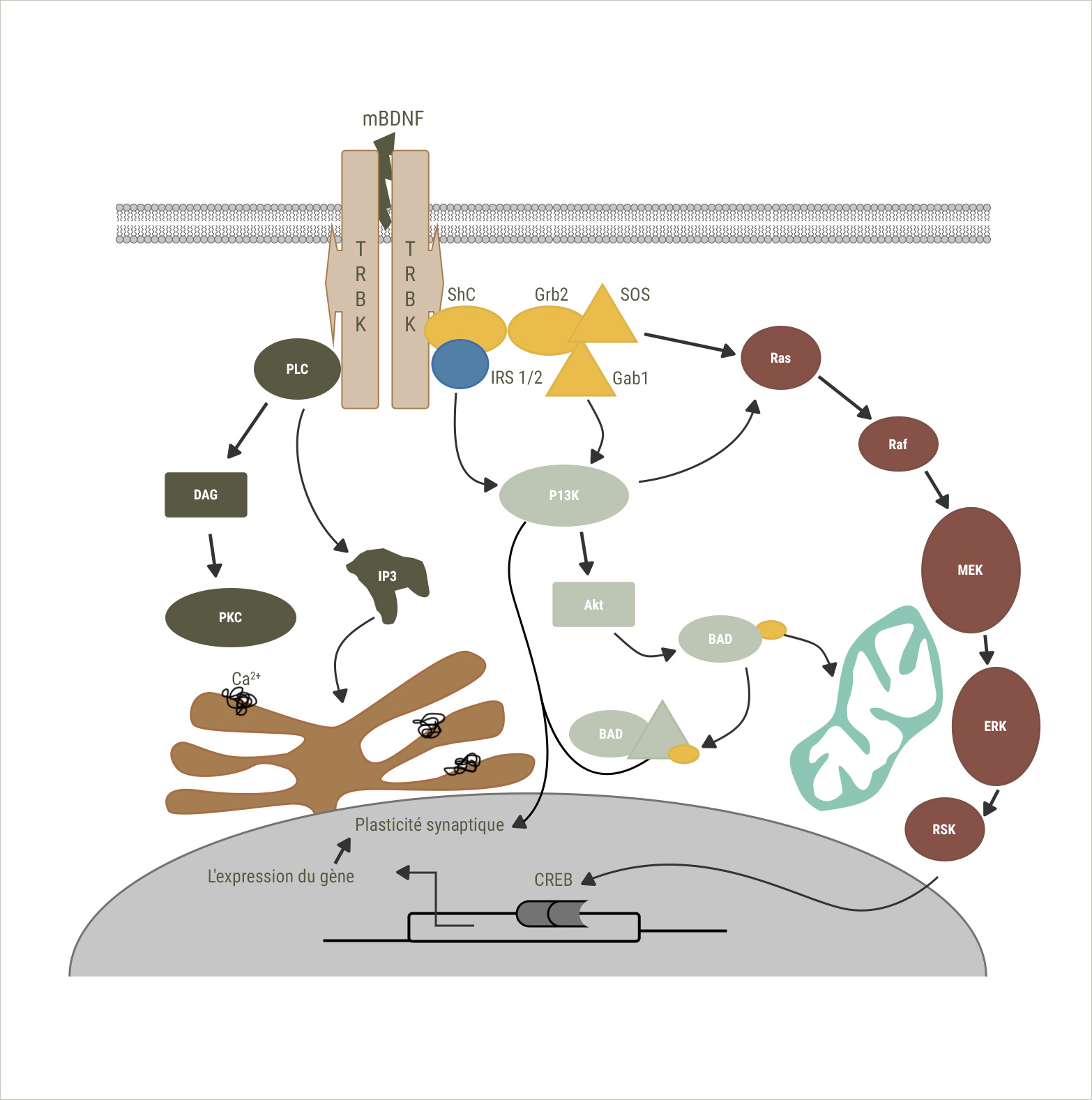
Baisse du taux de BDNF et altération de la santé cérébrale
Les niveaux de BDNF circulant dans l’organisme ont tendance à baisser au cours du vieillissement. Cette raréfaction est associée à une réduction du volume de l’hippocampe et à la survenue de problèmes de mémoire. Ses niveaux sont par ailleurs abaissés dans le cadre de la plupart des maladies neurodégénératives et chez les personnes atteintes de dépression. Il apparaît ainsi fondamental de maintenir des niveaux satisfaisants de ce composé pour conserver sa santé cérébrale.
Les myokines boostent la production du BDNF
Plusieurs myokines apparaissent en mesure de stimuler la production du BDNF au niveau du cerveau. Le BDNF est lui-même considéré comme une myokine, car les muscles en activité sont en mesure de le produire. Toutefois, il n’est pas libéré dans la circulation sanguine ; il ne peut agir que localement, apportant des bienfaits spécifiques au muscle.
L’action neuroprotectrice de l’irisine
L’irisine est l’une des principales myokines jouant un rôle anti-âge sur le cerveau. Lors d’un exercice physique, elle est libérée du muscle à partir d’une protéine appelée FNDC5 et déversée dans la circulation sanguine. Elle franchit la barrière hémato-encéphalique et vient s’ajouter au stock d’irisine produite au sein même de l’organe sous l’effet de l’exercice.
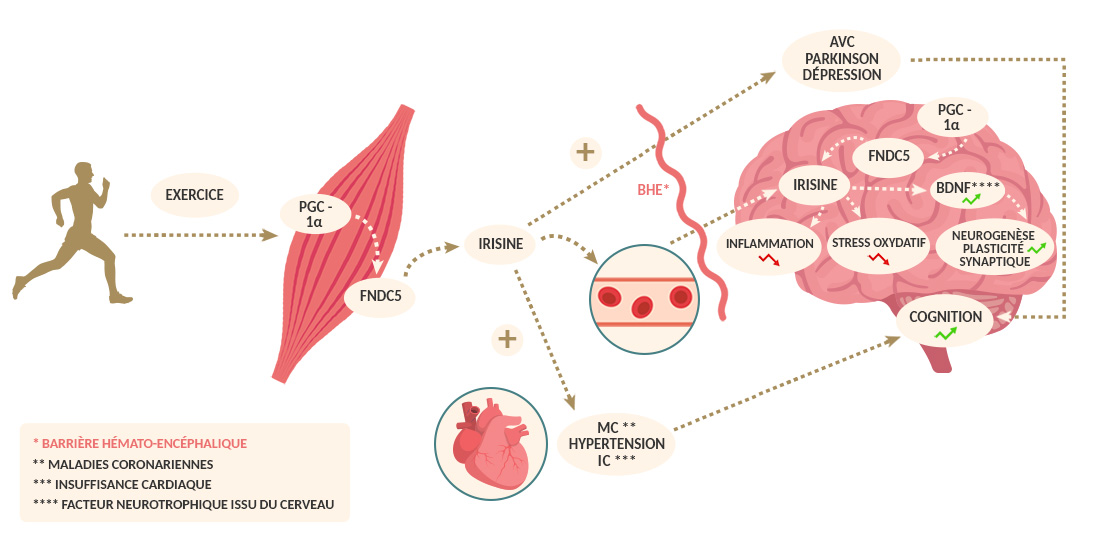
Une équipe s’est récemment intéressée à son potentiel effet protecteur dans le cadre de la maladie d’Alzheimer. Chez les malades, la quantité d’irisine présente au niveau du liquide dans lequel baigne le cerveau est plus faible que chez les personnes en bonne santé cérébrale.
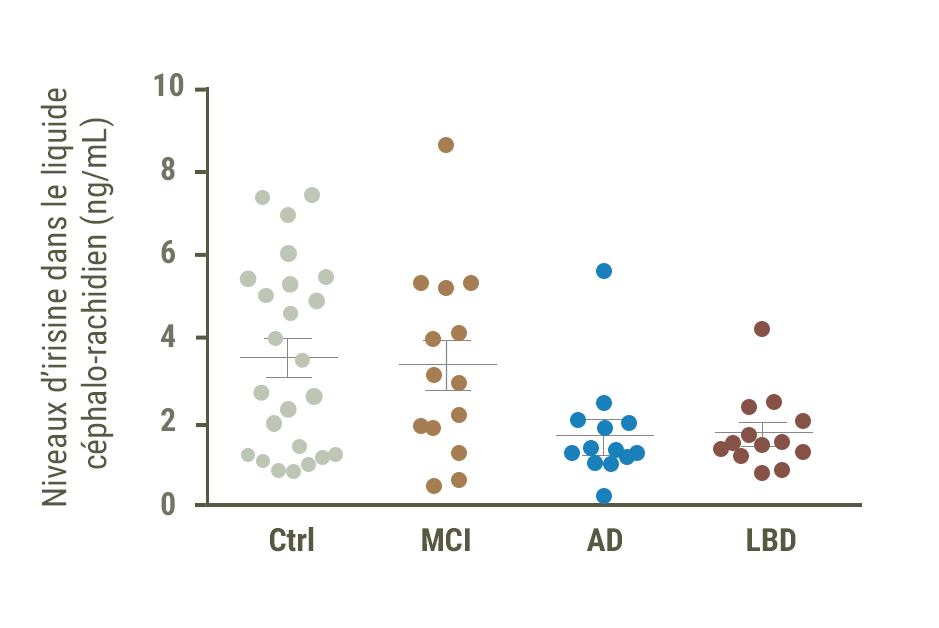
Les chercheurs ont utilisé un modèle animal de souris de la maladie d’Alzheimer pour mieux cerner l’action de la myokine. Ces souris présentent elles aussi un déficit en irisine au niveau du cerveau. Lorsqu’il a été corrigé par un apport direct au niveau de l’hippocampe, leurs problèmes de mémoire se sont améliorés. Les mêmes bienfaits ont été observés lorsque l’irisine a été administrée dans la circulation sanguine, confirmant la capacité de la myokine à franchir la barrière hémato-encéphalique et à agir sur la sphère cérébrale.
Une étude conduite auprès de 50 femmes de plus de 65 ans a montré que l’entraînement de résistance, à raison de deux sessions d’une heure par semaine pendant 12 semaines, est un bon moyen d’élever le taux d’irisine circulant dans l’organisme.
La cathepsine B améliore la cognition
Les effets bienfaisants du sport sont également relayés par la cathepsine B. Son absence, cumulée à celle d’une autre cathepsine (la cathepsine L), se traduit par un degré spectaculaire d’atrophie du cerveau.
Des travaux ont montré que les niveaux de cathepsine B augmentent dans le muscle et dans le sang chez des souris soumises à une activité de course. En réponse, la formation de nouveaux neurones est stimulée dans l’hippocampe des animaux, dont la mémoire spatiale s’améliore.
Tout du moins chez ceux sensibles à l’action de la cathepsine B : dans une lignée de souris privées de son action suite à une manipulation génétique, le sport ne peut pas remplir son rôle positif sur le cerveau. Grâce à des expériences sur des cultures de cellules souches neurales, les chercheurs ont pu prouver que les effets de la cathepsine B passent par la stimulation de la production du BDNF.
La dernière étape de leur étude a consisté à vérifier que ces résultats sont transposables chez l’homme. Des volontaires ont suivi un entraînement de 4 mois consistant en des séances de course sur tapis. À l’issue de cette période, la concentration en cathepsine B s’est élevée, avec des bénéfices notables sur la mémoire.
Les sports d’endurance ne sont pas les seuls à exercer cette influence positive sur le taux de cathepsine B. Des chercheurs ayant mené un essai clinique comparant l’entraînement aérobie et de résistance indiquent :
« Il est suggéré que l’exercice de résistance est plus efficace pour améliorer la concentration du sérum en BDNF et en cathepsine B, en raison d’une activité de contraction musculaire plus importante que l’exercice aérobie ».
Kun-Yong Sung et al.
Les corps cétoniques complètent l’action des myokines
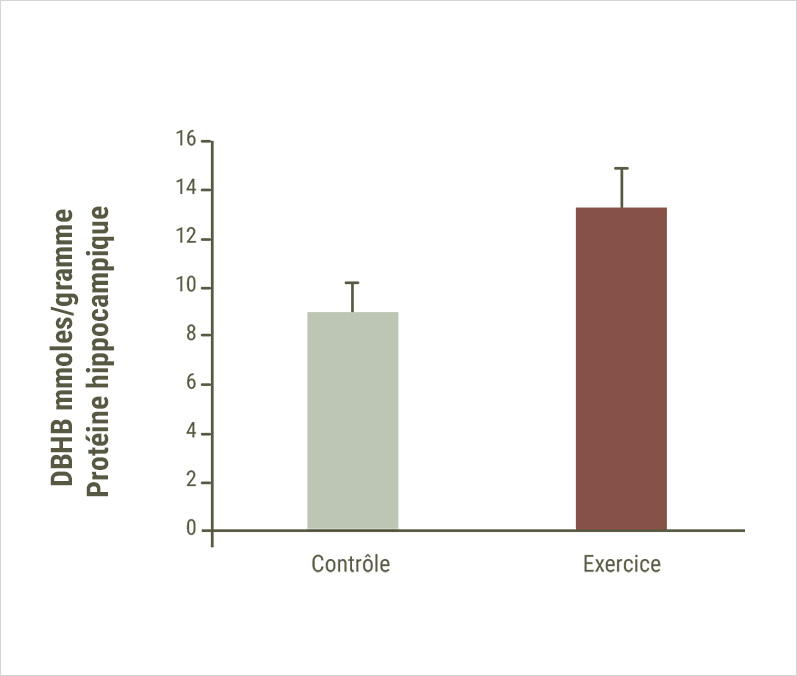
Un autre type de composés contribue aux effets favorables du sport sur le cerveau. Il s’agit du β-hydroxybutyrate (BHB), un corps cétonique produit par le foie à partir des acides gras quand le glucose vient à manquer, et utilisé comme source d’énergie alternative. Déversé dans la circulation sanguine, il est capable d’atteindre le cerveau.
Lors d’une étude chez la souris, des chercheurs ont montré que le BHB s’accumule au niveau de l’hippocampe des animaux après une course et ont mis en lumière ses effets.
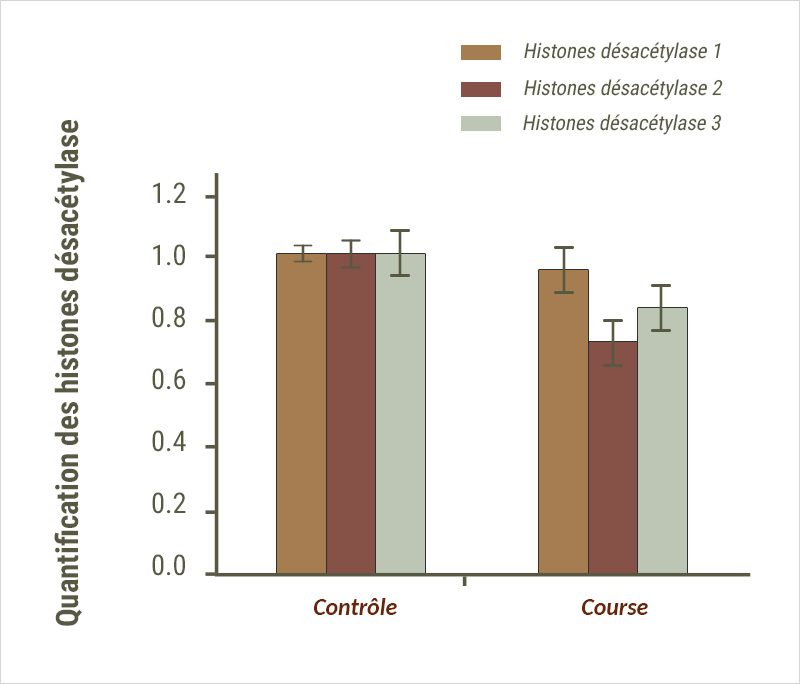
Le BHB s’oppose à l’action de certaines enzymes, les histones désacétylases (HDAC) 2 et 3. Les histones sont des protéines autour desquelles l’ADN s’enroule pour former une structure compacte appelée chromatine. Les HDAC sont responsables de la suppression de groupements chimiques acétyle au niveau des queues des histones. Elles maintiennent de cette manière la compaction de la chromatine, qui empêche l’expression des gènes. Comme le BHB inhibe leur action, cette entrave est levée et l’ADN devient accessible. Cette action permet notamment de relancer la production de BDNF.
L’administration de BHB, amorcée en milieu de vie chez des rats, permet ainsi d’améliorer les capacités d’apprentissage et les performances de la mémoire de travail au cours du vieillissement. Elle exerce également des effets neuroprotecteurs sur des modèles animaux de maladie de Parkinson et de Huntington.
À ce jour, les données chez l’être humain sont encore rares. Une étude a évalué les effets d’un entraînement avec des bandes élastiques, trois jours par semaine pendant 1h, sur 4 semaines chez des personnes âgées. Chez les participants qui présentaient un niveau sanguin faible de BHB avant l’entraînement, le taux s’est amélioré sous l’effet de l’activité physique. Une légère association positive entre le taux de BHB et les fonctions cognitives est alors apparue.
Autres articles



